Endowiki: aggiornamento continuo di endocrinologia
Per tutti gli operatori di endocrinologia: lo stato dell'arte su clinica e terapia.
Uno strumento semplice e fruibile da tutti coloro che intendono essere sempre aggiornati, promosso dai migliori operatori del settore.
News
Anatomia della tiroide e corrispondenza con imaging e chirurgia
Pierpaolo Trimboli
Servizio di Endocrinologia e Diabetologia, Ospedale Israelitico di Roma
ANATOMIA
Forma e posizione
La tiroide è costituita da due lobi laterali, uniti da un istmo mediano. I due lobi hanno forma conica, e si estendono da metà altezza della cartilagine tiroidea fino al quinto anello tracheale. Hanno una lunghezza di circa 3 cm, uno spessore che varia da 0.5 cm dell’apice a 2 cm della base. L’istmo unisce i due lobi in prossimità della loro base, all’altezza dei primi due anelli tracheali. Dal margine superiore dell’istmo può dipartire verso l’alto un prolungamento ghiandolare di lunghezza variabile, che prende il nome di lobo piramidale. Esso rappresenta una testimonianza del percorso compiuto dalla ghiandola durante il suo sviluppo embrionale. Le dimensioni complessive della tiroide variano molto a seconda dell’età e del sesso.
Rapporti
La tiroide è applicata sulla superficie ventrale della laringe e dei primi due anelli tracheali, parzialmente coperta dai muscoli sternocleido-mastoideo, sterno-tiroideo e omoioideo, e dalla fascia cervicale media. La ghiandola si trova all’interno di una guaina fibrosa (guaina tiroidea), attraverso la quale è in contatto con gli organi circostanti. Posteriormente alla guaina tiroidea dipartono tralci connettivali che assicurano l’organo alla laringe (legamento sospensore), alla cartilagine laringea e ai primi anelli tracheali (legamenti laterali interni), e alla guaina che circonda il fascio vascolo-nervoso del collo (legamenti laterali esterni). Posteriormente, il lobo sinistro è inoltre in contatto con il tubo faringo-esofageo, dove decorre il nervo laringeo inferiore. La ghiandola è ricoperta dall’interno all’esterno dalla propria guaina connettivale, dallo spazio pericoloso tiroideo (un intreccio di arterie e vene dell’organo) e dalla guaina peri-tiroidea.
Vasi e nervi
La tiroide è irrorata dalle arterie tiroidee superiori destra e sinistra, rami delle carotidi comuni esterne, e dalle arterie tiroidee inferiori destra e sinistra, rami del tronco tireo-cervicale della succlavia. A volte è presente l’arteria tiroidea ima, ramo dell’arteria brachi-cefalica oppure della carotide comune, che raggiunge dal basso l’istmo. I rami di divisione dell’arteria tiroidea inferiore sono in stretto contatto con il nervo laringeo inferiore (o ricorrente), ramo del nervo vago.
Le vene reflue dal circolo intra-tiroideo formano un plesso nello spazio pericoloso, da cui originano le vene tiroidee superiori destra e sinistra (tributarie della vena giugulare interna omolaterale) e inferiori destra e sinistra (tributarie della vena brachio-cefalica omolaterale).
I vasi linfatici sono tributari della catena giugulare interna (verso l’alto) e dei linfonodi para-tracheali e pre-tracheali (verso il basso).
La tiroide riceve nervi dal simpatico cervicale e dai due nervi laringei del nervo vago.
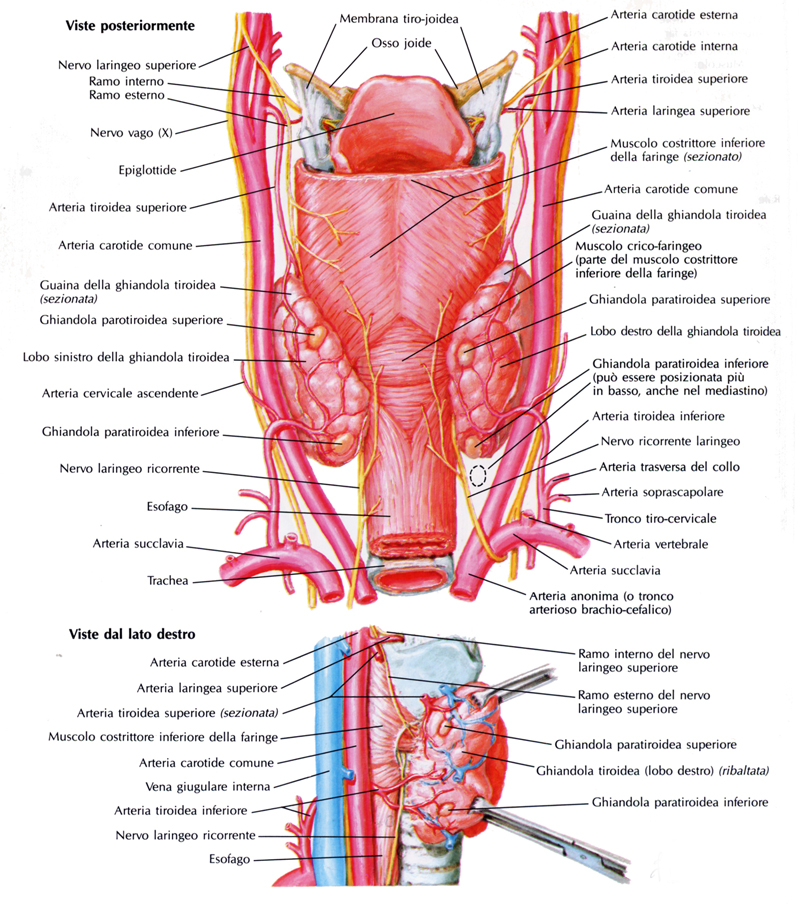
Figura 1. Rappresentazione di vasi e nervi della tiroide.
Struttura
La ghiandola tiroidea è suddivisa in lobuli, formati da esili tralci che si dipartono dalla capsula connettivale. I vasi e i nervi raggiungono le singole unità funzionali con i tralci connettivali.
Follicoli tiroidei. La tiroide ha una organizzazione follicolare. È costituita infatti da una serie di vescicole (follicoli tiroidei) con una parete (l’epitelio follicolare). L'epitelio follicolare è formata da uno strato singolo di cellule follicolari (o tireociti), e costituisce una cavità all’interno della quale si ritrova un materiale amorfo (colloide). I tireociti sono responsabili della sintesi e immissione in circolo dei due ormoni tiroidei, T3 e T4. Le dimensioni dei follicoli variano molto a seconda dello stato funzionale. In una condizione di ipofunzionalità si riscontrano facilmente macrofollicoli, con una cavità molto dilatata ripiena di colloide. I follicoli con questo atteggiamento non contribuiscono a fornire ormoni circolanti, ma costituiscono una forma di riserva di ormoni. I tireociti sono caratterizzati da una doppia polarità: nella fase di sintesi operano sul lato luminale accumulando colloide, nella fase di immissione ormonale in circolo operano sul versante opposto. Nella prima fase viene prodotta una glicoproteina (tireoglobulina) in parte nel reticolo endoplasmatico e in parte nell’apparato di Golgi. Oltre alla tireoglobulina, le vescicole contengono un enzima ossidativo (perossidasi tiroidea) che ossida gli ioduri che i tireociti captano dal sangue. Nella fase di immissione di ormoni in circolo la membrana cellulare forma estroflessioni che attorniano gocciole di colloide e per fagocitosi le introducono all’interno del tireocita, ricco in questa fase di fagosomi. Con la formazione di complessi di fagolisosomi avviene la scissione degli ormoni tiroidei, e quindi la loro emissione.
Cellule parafollicolari o cellule C. Oltre ai tireociti, la tiroide possiede un altro tipo cellulare (cellule parafollicolari, o cellule C), intercalate tra i tireociti o sparse nell’interstizio tra i follicoli. Sono voluminose cellule a citoplasma chiaro, presenti sulla membrana basale del follicolo, ma sprovviste di una faccia luminale. Queste cellule sono facilmente riconoscibili al microscopio elettronico per la presenza di un reticolo endoplasmatico rugoso meno evidente e di un apparato di Golgi peri-nucleare. Il loro citoplasma contiene numerose vescicole di secrezione. Le cellule C producono la calcitonina, un polipeptide di 32 aminoacidi, accumulato all’interno di vescicole di secrezione insieme a serotonina e somatostatina.
Linfonodi del collo di interesse tiroideo
I linfonodi del collo possono essere classificati, in base alla loro sede, in sei livelli, dall'alto verso il basso. Il VII livello è costituito dai linfonodi del mediastino alto. Tutti i livelli possono essere sede di ripetizione metastatica di tumori a partenza da varie strutture della testa, del collo, dell'addome superiore e del torace (Figura 2). I linfonodi di interesse nella patologia tumorale tiroidea sono principalmente quelli del III e IV omolaterali con il lobo tiroideo sede del tumore primario, e quelli del VI livello (compartimento centrale). Meno frequentemente vengono compromessi anche quelli del V livello (sovraclaveari), omolateralmente con il tumore. Talvolta anche i linfonodi del VII livello possono essere sede di metastasi da tumori differenziati della tiroide. Questi ultimi risultano non valutabili ecograficamente.
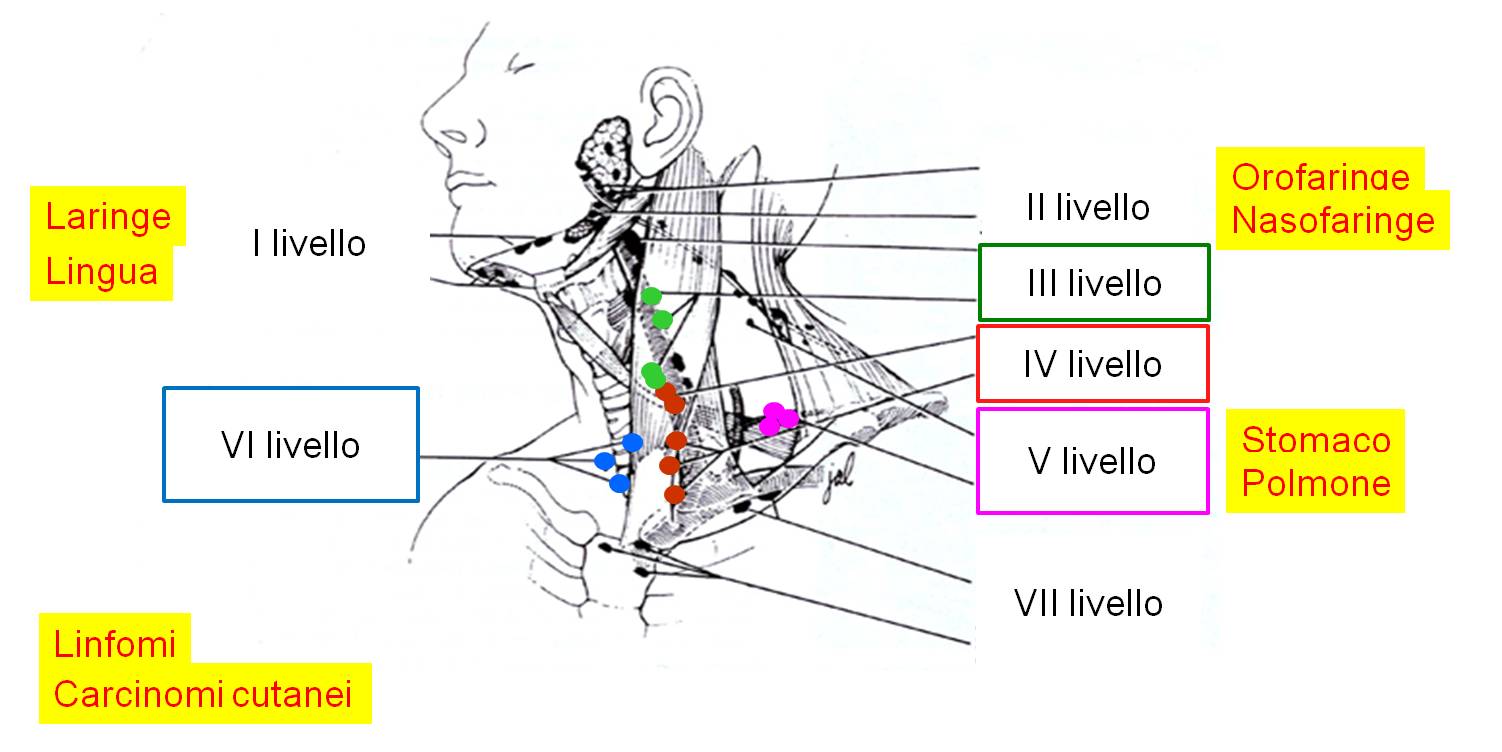
Figura 2. Rappresentazione schematica della anatomia dei linfonodi del collo di interesse tiroideo. I livelli interessati da possibili metastasi tiroidee sono, in ordine di frequenza, VI, IV, III, V, II e I. In giallo sono evidenziati gli altri organi in grado di dare metastasi cervicali.
Bibliografia
1. Trattato di Anatomia Umana. Ed. edi-ermes. Cap 13 (vol II).
CORRISPONDENZA TRA ANATOMIA ED ECOGRAFIA TIROIDEA
Sulla base delle conoscenze anatomiche, l’ecografia rappresenta il miglior metodo di valutazione della morfologia tiroidea. La densità ecografica della ghiandola tiroidea si presenta tipicamente superiore (iperecogena) rispetto alle strutture vicine, e questo la rende facilmente visualizzabile (figura 3). La visualizzazione della tiroide consente di valutare le dimensioni dei due lobi e il volume della ghiandola, i suoi profili, l’omogeneità e l’ecogenicità della sua struttura, l'eventuale presenza di noduli palpabili e non.
La tiroide in condizioni normali si presenta con profili regolari, con ecostruttura omogenea ed ecogenicità conservata, cioè come detto iperecogena rispetto alle strutture circostanti. L’omogeneità del tessuto è legata alla normale organizzazione follicolare, mentre l’ecogenicità si associa al normale rapporto tra cellule e colloide.
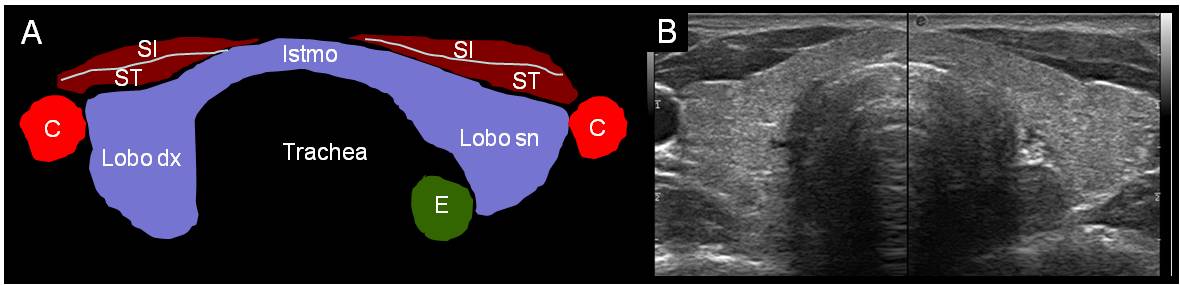
Figura 3. Corrispondenza fra strutture anatomiche e visualizazione ecografica in sezione trasversa (C = carotide, SI = muscolo sterno-ioideo, ST = muscolo sterno-tiroideo, E = esofago)
Alterazioni ecografiche ghiandolari
Diversi studi hanno dimostrato come un quadro ecografico tiroideo con ecostruttura disomogenea ed ecogenicità ridotta si associ a condizioni di tiroidite cronica e/o ipotiroidismo istologicamente dimostrabili (1-3). In una tiroide con tale aspetto, l’ecostruttura è disomogenea per sofferenza ghiandolare, e l’ecogenicità è ridotta a causa dell’alterato rapporto colloide/cellule a favore delle cellule, in questo caso di tipo infiammatorio. Al contrario, pochi studi hanno analizzato l’associazione tra ecostruttura ed ecogenicità normali e funzione tiroidea. Un recente lavoro, non di popolazione, indica come il 20% circa dei soggetti adulti con tiroide ecograficamente normale presenterebbe un’alterazione biochimica tiroidea (4). Tuttavia, queste alterazioni di laboratorio potrebbero non avere un reale significato clinico, e si può ipotizzare che una tiroide normale all’esame ecografico presenti una normale funzione e negatività sierica di anticorpi anti-tiroidei. Studi basati sulla popolazione sarebbero necessari per chiarire questi aspetti. Per quanto riguarda infine la corrispondenza tra stima ecografica del volume tiroideo e anatomia, non esistono ad oggi studi che abbiano chiarito quale sia il normale volume ghiandolare in un soggetto adulto. Diversi autori riportano invece come in soggetti in età infantile o adolescenziale il volume tiroideo aumenti con l’aumentare dell’età e del peso corporeo.
Classificazione ecografica dei noduli e corrispondenza anatomica
I noduli tiroidei si presentano ecograficamente come lesioni focali, con ecostruttura ed ecogenicità variabili in base alla diversa struttura tissutale. Generalmente i noduli tiroidei possono essere distinti ecograficamente in solidi, isoecogeni o ipoecogeni, misti con quote solide più o meno prevalenti, o anecogeni e privi di aree solide. Questa sommaria classificazione ecografica ha una buona corrispondenza con l’anatomia nodulare solo in alcuni casi.
- Nei noduli isoecogeni, definiti tali perchè l'ecogenicità è non dissimile dal tessuto ghiandolare sano circostante, è conservato il rapporto colloide/cellule.
- I noduli ipoecogeni, definiti tali quando l'ecogenicità è inferiore al tessuto ghiandolare sano circostante, hanno invece un aumento della quota cellulare rispetto alla colloide. La scarsa colloide e l'abbondante cellularità è una caratteristica tipica delle neoplasie tiroidee sia citologicamente che istologicamente.
- Riguardo la struttura nei noduli misti c'è una preponderanza della quoata liquida ed una quota solida variabile mentre i noduli cistici (anecogeni) sono completamente liquidi o quasi.
Gli apparecchi ecografici di ultima generazione permettono la valutazione delle caratteristiche dei margini nodulari. In alcuni casi è possibile evidenziare un'irregolarità dei margini e questo rappresenta una caratteristica ecografica di forte sospetto. Non sono ad oggi disponibili studi che analizzino la corrispondenza istologica di noduli con margini classificati ecograficamente come irregolari (figura 4).
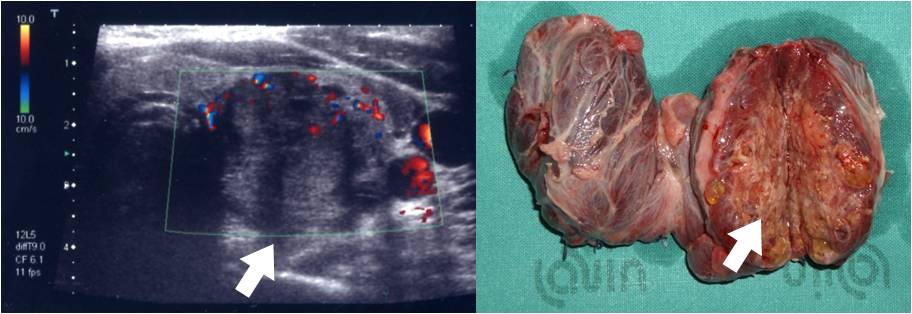
Figura 4. Nodulo tiroideo del lobo sinistro ghiandolare. Il nodulo si presenta all'ecografia solido, ipoecogeno, con margini irregolari (segni di invasione) e lievi cenni di vascolarizzazione. Dopo l'escissione chirurgca si può notare la corrispondenza del quadro ecografico con la valutazione macroscopica dell'irregolarità dei margini nodulari.
Bibliografia
- Rago T, Chiovato L, Grasso L, et al. Thyroid ultrasonography as a tool for detecting thyroid autoimmune diseases and predicting thyroid disfunction in apparently healthy subjects. J Endocrinol Invest 2001, 24: 763-9.
- Marcocci C, Vitti P, Cetani F, et al. Thyroid ultrasonography helps to identify patients with diffuse lymphocytic thyroiditis who are prone to develop hypothyroidism. J Clin Endocrinol Metab 1991, 72: 209-13.
- Rago T, Di Coscio G, Ugolini C, et al. Clinical features of thyroid autoimmunity are associated with thyroiditis on histology and are not predictive of malignancy in 570 patients with indeterminate nodules on cytology who had a thyroidectomy. Clin Endocrinol (Oxf) 2007, 67: 363-9.
- Trimboli P, Rossi F, Thorel F, et al. One in five subjects with normal thyroid ultrasonography has altered thyroid tests. Endocr J 2012, 59: 137-43.
Lo iodio e i disordini da carenza iodica
Pierpaolo Trimboli
Servizio di Endocrinologia e Diabetologia, Ospedale Israelitico di Roma
Lo iodio è un oligoelemento scarsamente rappresentato in natura. Anche nell'organismo umano si ritrovano piccole quantità di iodio. L’acqua e gli alimenti rappresentano la fonte principale di apporto iodico per l'uomo, mentre lo iodio inalato (per es. in prossimità del mare) costituisce soltanto una quota minima del fabbisogno iodico giornaliero. Una volta ingerito, lo iodio viene assorbito dall’intestino e trasportato nei tessuti che hanno la possibilità di captarlo. La principale sede di utilizzo è la tiroide che lo impiega per la sintesi degli ormoni tiroidei T3 e T4. Un adeguato apporto di iodio è, infatti, essenziale per la normale funzione tiroidea e per la fisiologica crescita e sviluppo dei diversi organi e apparati che risentono dell’azione degli ormoni tiroidei. La principale via di escrezione dello iodio (98%) è quella renale, tanto che l’apporto iodico si valuta attraverso la determinazione della concentrazione (μg/L) dello iodio urinario (ioduria), esame ancora non di largo impiego.
L’apporto giornaliero raccomandato di iodio è in stretta relazione al suo fabbisogno, che varia nell’arco della vita in funzione delle diverse condizioni fisiologiche (tabella 1).
| Tabella 1 Fabbisogno giornaliero di iodio (in µg/die) |
||
| Età | Raccomandato | Massimo |
| 0-7 anni | 90 | 200 |
| 8-12 anni | 120 | 600 |
| Adulti | 150 | 600 |
| Gravidanza ed allattamento | 250 | 600 |
Sulla base della ioduria è possibile classificare l'apporto iodico della popolazione (tabella 2).
| Tabella 2 Classificazione dell’apporto iodico |
|
| Ioduria (mediana) µg/L | Classificazione |
| < 20 | Deficit severo |
| 20-49 | Deficit moderato |
| 50-99 | Deficit lieve |
| 100-199 | Ottimale |
| 200-299 | Più che ottimale |
L’Italia, come gran parte dell’Europa, è stata classificata paese a carenza iodica lieve, con differenze tra il Nord ed il Sud (al 2009 la ioduria era, rispettivamente, di 98 µg/L vs 79 µg/L). La carenza iodica deve essere eradicata con l’uso del sale fortificato con iodio (in Italia il sale è addizionato con iodato di potassio nella misura di 30 mg/kg sale, pari a 30 µg/g di sale) (1).
Le malattie da deficit dell’apporto iodico (IDD, Iodine Deficiency Disorders)
L’insufficiente apporto iodico alimentare determina una serie di manifestazioni cliniche, denominate malattie da deficit dell’apporto iodico (IDD, Iodine Deficiency Disorders), che si manifestano, a seconda della gravità, della durata e del periodo di esposizione alla carenza iodica con vari quadri clinici:
- nel feto: aborti, natimortalità, anomalie congenite
- nel neonato: aumento della mortalità perinatale, gozzo, ipotiroidismo, cretinismo (neurologico e mixedematoso), ritardato sviluppo psicomotorio e mentale
- nell’adolescente: gozzo, ipotiroidismo giovanile, variabile ritardo mentale, ritardo dell’accrescimento, aumentata suscettibilità alle radiazioni.
La manifestazione clinica più evidente e frequente della carenza iodica è il gozzo, cioè l’aumento di volume della tiroide non riferibile a processi flogistici o neoplastici. È più frequente nel sesso femminile (F/M= 9/1), e durante la pubertà e la gravidanza.
Per la diagnosi delle IDD, è fondamentale la raccolta dei dati anamnestici, con particolare attenzione all’età, alla familiarità, alla zona di provenienza e di residenza del paziente e alle abitudini alimentari. Segue l’esame obiettivo della regione anteriore del collo e la diagnosi strumentale che si avvale principalmente dell’ecografia tiroidea. Gli esami di laboratorio necessari sono: TSH, FT3, FT4, ioduria. Quest’ultimo è utilizzato specialmente nelle indagini epidemiologiche ed in condizioni particolari quali la gravidanza e l’allattamento, in cui è necessario accertare che venga soddisfatta l’aumentata richiesta di apporto iodico. La gravidanza rappresenta infatti una condizione fisiologica in cui la tiroide va incontro ad un adattamento funzionale. Durante la gestazione, infatti, si verificano quattro eventi che determinano un aumentato fabbisogno giornaliero di iodio: aumentata clearance renale, passaggio di iodio transplacentare, incremento di captazione da parte della tiroide, aumentata richiesta periferica di ormone tiroideo (2). In considerazione di queste modificazioni a carico del metabolismo dello iodio che si verificano nel corso della gravidanza, risulta dunque importante monitorare l’apporto iodico ed eventualmente correggerne una condizione di carenza (3).
In età adolescenziale a volte il sintomo predominante della carenza iodica è la ridotta velocità di crescita staturale: questo perché il deficit di ormoni tiroidei provoca sia la diminuita secrezione di GH, sia il suo minore effetto sulla cartilagine di accrescimento.
Per i quadri di ipotiroidismo si rinvia al relativo capitolo.
Bibliografia
- Panunzi C. Gozzo e deficit iodico. In: Manuale per la valutazione e l'inquadramento delle patologie della tiroide. AME 2011.
- Glinoer D. The regulation of thyroid function during normal pregnancy: importance of the iodine nutrition status. Best Pract Res Clin Endocrinol Metab 2004, 18: 133-52.
- The Public Health Committee of the American Thyroid Association. Iodine supplementation for Pregnancy and Lactation - United States and Canada: Recommendations of the American Thyroid Association. Thyroid 2006, 16: 949-51.